
¿Qué es la molalidad?
La molalidad se define como los «moles totales de un soluto contenidos en un kilogramo de disolvente».
La molalidad también se conoce como concentración molal. Es una medida de la concentración de soluto en una solución. La solución se compone de dos componentes; soluto y solvente. Hay muchas formas diferentes de expresar la concentración de soluciones como molaridad, molalidad, normalidad, formalidad, porcentaje en volumen, porcentaje en peso y partes por millón. El término necesita calcular la masa del solvente y los moles de soluto.
Fórmula de molalidad
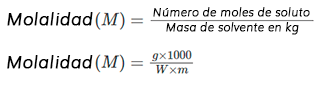
Diferencia entre molaridad y molalidad
| Molalidad | Molaridad |
| Masa del solvente | Volumen de toda la solución |
| Signo unitario expresado como (m) | Signo unitario expresado como (M) |
| Tiene unidades de moles/kg | Tiene unidades de moles/litro |
Ejemplos de molalidad
Pregunta: Calcule la molalidad de una solución donde se disuelven 5.0 gramos de tolueno (C7H8) en 225 gramos de benceno (C6H6). Calcular los moles del soluto dado.
Solución:
Tolueno: Peso molecular = C7H8 = (7 x 12) + (1 x 8) = 92 gramos/mole
Usando la fórmula:
Moles de tolueno = Masa en gramos / peso molecular = 5.0 gramos / 92 gramos/mole = 0.054 mole
Entonces el mol de tolueno es
0.054 mole.
Ahora calcula el kilogramo de disolvente.
225 gramos de benceno / 1000 = 0.225 kilogramos
Como paso final, calcula la molalidad usando la fórmula.
Molalidad (m) = Moles de Tolueno / Masa de Benceno en gramos
Molalidad (m) = 0.054 moles / 0.225 kg
Molalidad (m) = 0.24 m
Preguntas Frecuentes
La molaridad es el número de moles de una sustancia por litro de solución, también conocida como concentración molar. Una M mayúscula significa soluciones etiquetadas con concentración molar. Una solución 1.0 M contiene 1 mol de disolvente por litro de solución. La molalidad es el número de moles de disolvente por kilogramo.
La molalidad es una propiedad de la solución y se define como el número de moles de disolvente por kilogramo. La unidad de molalidad en el SI es mol/kg. Una solución con una molalidad de 3 molar/kg a menudo se define como “3 molal” o “3 m”. Sin embargo, ahora se prefiere seguir la unidad del sistema SI, mol/kg o una unidad SI similar.
La molalidad es el método de transmisión de concentración preferido porque la masa de soluto y disolvente de la solución no cambia.
Es mejor realizar pruebas prácticas en un laboratorio. Aunque debido a las diferencias de temperatura que afectan el volumen en molaridad y no en molalidad, no es tan confiable como la molalidad. Las fuentes de error de molaridad provenientes de la estimación de volumen también son mayores que los errores de un balance de molalidad.
La molaridad (M) es una de las unidades más comunes utilizadas para cuantificar la concentración de una solución, representando el número de moles de soluto por litro de solución (moles/litro).
Para obtener más información sobre la molaridad y otros temas relacionados, ingresa a UnaEnergia.com.
