
Las emulsiones son las mezclas de dos o más tipos de líquidos en las que, uno de ellos es como gotitas de tamaño minúsculo o incluso ultramicroscópico, que se distribuyen entre sí. Suelen formarse a partir del componente de los líquidos de forma natural o, más a menudo, utilizando mecanismos, como la agitación, siempre que estos fluidos mezclados no tengan ningún tipo de solubilidad mutua.
Se dice que las emulsiones están estabilizadas por algunos agentes que forman películas en la superficie de las gotas o que les confieren una especie de estabilidad mecánica. La forma inestable de las emulsiones eventualmente se separa en dos formas de capas líquidas. Las emulsiones estables se destruyen desactivando el agente emulsionante, por ejemplo, mediante la adición de sustancias de terceros apropiadas o incluso mediante el proceso de congelación o calentamiento.
Algunas emulsiones comunes son la leche (que es la dispersión de moléculas o gotitas de grasa en la solución acuosa) y también la mantequilla (que es la dispersión de gotitas de partículas de una solución acuosa en la grasa).
¿Qué es una Emulsión?
Una emulsión puede definirse como un coloide formado por dos o más tipos de líquidos no homogéneos en el que uno de los líquidos contiene la dispersión de las diferentes formas de líquidos.
Ejemplos de Emulsiones
Las emulsiones consisten básicamente en la dispersión de dos líquidos inmiscibles entre sí. Uno de los líquidos actuará como medio de dispersión y el otro como fase dispersa. En palabras sencillas, las emulsiones son coloides en los que tanto la fase dispersa como el medio de dispersión son líquidos. El aceite y las mezclas de agua son emulsiones cuando se agitan juntos. El aceite forma una gota y luego se dispersa por el agua.
El término emulsión también se aplica a un grupo de sistemas mezclados llamados soluciones o geles, o suspensiones. Por ejemplo, la emulsión fotográfica es un gel de gelatina formado por pequeños cristales dispersos en ella. Otros ejemplos de emulsiones son la mantequilla, que es una emulsión de agua en grasa, y la yema de huevo que contiene lecitina.
| FASE DISPERSA | MEDIO DE DISPERSIÓN | TIPO DE COLOIDE | EJEMPLO |
| Sólido | Sólido | Sólido | Algunos cristales de colores y piedras preciosas |
| Sólido | Líquido | Sólido | Pinturas, Fluidos Celulares |
| Sólido | Gas | Aerosol | Humo, Polvo |
| Líquido | Sólido | Gel | Queso, Mantequilla, Gelatinas |
| Líquido | Líquido | Emulsión | Leche, Crema para el cabello |
| Líquido | Gas | Aerosol | Niebla, Neblina, Nube, Aerosoles Insecticidas |
| Gas | Sólido | Sólido | Piedra pómez, Gomaespuma |
| Gas | Líquido | Espuma | Espuma, Crema batida, Espuma de jabón |
Propiedades de las Emulsiones
- Las emulsiones son a la vez continuas y dispersas, con un límite entre las fases que se denominan «interfaz».
- Las emulsiones tienen un aspecto turbio debido a que muchas interfaces de fase dispersan la luz que pasa a través de las emulsiones.
- Las emulsiones aparecen en color blanco cuando la luz se dispersa en proporciones iguales.
- Si la emulsión está diluida, los tipos de luz de mayor frecuencia y menor longitud de onda se dispersarán en más fracciones, y este tipo de emulsión aparecerá en color azul. Esto también se conoce como efecto Tyndall.
Tipos de Emulsiones
Las emulsiones pueden clasificarse en función de las propiedades de la fase dispersa y del medio de dispersión.
- Aceite en agua: En este tipo de emulsión, el aceite será la fase dispersa y el agua será el medio de dispersión. El mejor ejemplo de emulsión aceite/agua es la leche. En la leche, los glóbulos de grasa (que actúan como fase dispersa) están suspendidos en agua (que actúa como medio de dispersión).
- Agua en aceite: En este tipo, el agua será la fase dispersa y el aceite será el medio de dispersión. La margarina (una pasta para untar utilizada para aromatizar, hornear y trabajar) es un ejemplo de emulsión de agua en aceite.
Emulsionante/Agente Emulsionante
Son sustancias que se añaden a las emulsiones con fines de estabilización. Las diversas características de los emulsionantes se dan a continuación:
- Son sustancias que tienen un extremo hidrofílico (polar) y otro hidrofóbico (no polar).
- Son solubles tanto en agua como en aceite.
- Los emulsionantes forman una capa entre la fase dispersa y el medio de dispersión, impidiendo así que las partículas de la fase dispersa se junten para formar partículas más grandes y se separen.
- Los emulsionantes pueden ser catiónicos, aniónicos o incluso apolares.
- No es sólo el porcentaje de agua y aceite lo que decide si se trata de una emulsión de aceite en agua o de agua en aceite. Por el contrario, depende de qué agua y aceite puedan disolver en mayor medida el emulsionante.
- Si el emulsionante es más soluble en agua, el agua se convierte en el medio de dispersión y el aceite en la fase dispersa, por lo que obtenemos una emulsión de aceite en agua.
- Por otro lado, si el emulsionante es más soluble en aceite, entonces el aceite se convierte en el medio de dispersión y el agua en la fase dispersa.
- Los emulsionantes más utilizados para las emulsiones aceite/agua son proteínas, gomas, jabones, etc.
- Los emulsionantes más utilizados para las emulsiones agua/aceite son sales de metales pesados de ácidos grasos, alcoholes de cadena larga, etc.
Algunos ejemplos comunes de emulsionantes son la yema de huevo, la mostaza, los fosfatos sódicos, el DATEM, los mono- y diglicéridos, la celulosa, la lecitina de soja, etc.
¿Cómo Funcionan los Emulsionantes?
Para entender esto, en primer lugar, tenemos que comprender el proceso de coalescencia. La coalescencia es el proceso en el que partículas similares de las emulsiones se unen para formar partículas más grandes y voluminosas, lo que conduce a la separación de la fase dispersa y el medio de dispersión.
Los emulsionantes ayudan a evitar la coalescencia formando una barrera física entre la fase dispersa y el medio de dispersión. Como hemos visto antes, los emulsionantes, como el jabón, tienen un extremo hidrofílico y otro hidrofóbico. Por lo tanto, pueden adherirse a sustancias polares y no polares. Tomemos el ejemplo del estearato sódico. C17H35COO-Na puede representarse como,
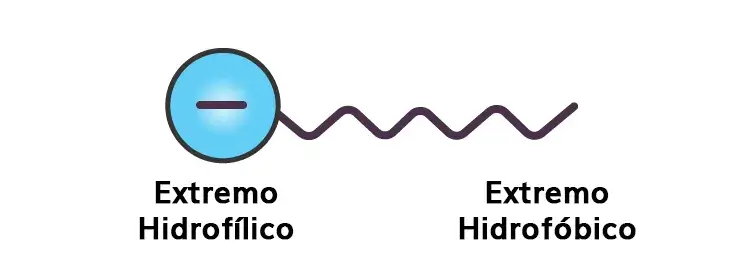
Cuando se añade a una emulsión aceite/agua, las moléculas de C17H35COO- rodean la gota de aceite con sus colas no polares/extremo hidrofóbico (la cadena de hidrocarburos), extendiéndose hacia el interior del aceite y sus cabezas polares/extremo hidrofílico (el ion carboxilato), orientadas hacia el agua, tal como se muestra en la figura.
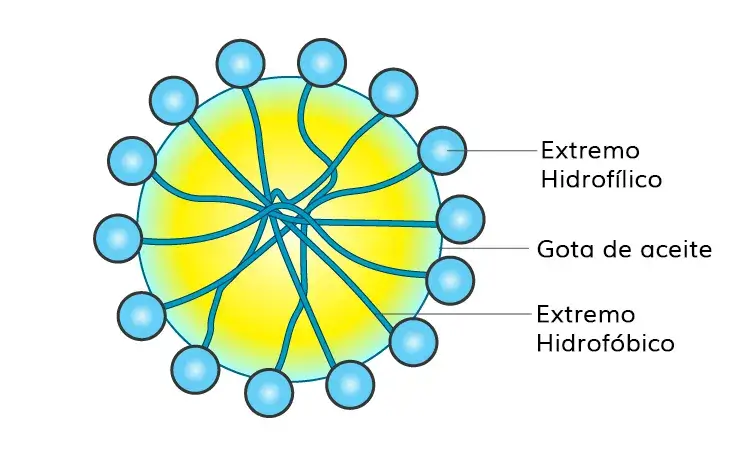
Esta disposición aporta una fuerza adhesiva más fuerte entre el aceite (fase dispersa) y el agua (medio de dispersión). Esta fuerza adhesiva recién formada será mayor que la fuerza de cohesión entre aceite-aceite y agua-agua. Por lo tanto, las partículas de aceite no tenderán a juntarse para formar partículas más grandes. Esto ayuda a evitar la coalescencia, estabilizando así la emulsión.
Nota:
Para la emulsión agua/aceite, la orientación del emulsionante sería la opuesta a la de aceite/agua, es decir, la cola no polar (extremo hidrofóbico) se extiende hacia fuera, y la cabeza polar (extremo hidrofílico) mira hacia dentro.
Teoría de las Emulsiones
Dado que en el proceso de emulsificación intervienen distintos procesos y mecanismos (tanto químicos como físicos), existen varias teorías que lo acompañan.
Teoría de la tensión superficial: Esta teoría establece o describe la emulsificación como un proceso que se produce por la reducción de la tensión interfacial entre dos fases.
Teoría de la repulsión: Con esta teoría, aprendemos que el agente emulsionante produce una película sobre una fase, lo que conduce además a la formación de glóbulos. Estos compuestos tienden a repelerse, y la fuerza repulsiva que existe entre ellos les ayuda a permanecer suspendidos en el medio de dispersión.
Métodos para Identificar el Tipo de Emulsiones
1) Prueba de dilución
Al añadir agua a una emulsión aceite/agua, ésta seguirá siendo estable, ya que el agua es el medio de dispersión, pero al añadir aceite se desestabilizará, ya que el aceite y el agua son inmiscibles. Del mismo modo, una emulsión agua/aceite puede diluirse con aceite y seguirá siendo estable, pero se desestabilizará al añadir agua.
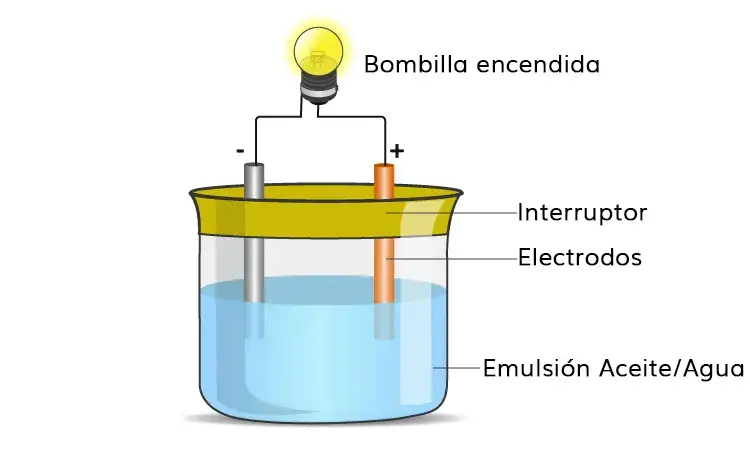
2) Prueba de conductividad
En esta prueba, la emulsión se mantiene entre 2 electrodos y se conecta una bombilla al circuito, como se muestra en el diagrama. Una emulsión aceite/agua conducirá la electricidad como lo hace el agua, pero un agua/aceite no la conducirá.
3) Prueba de tinte
En este caso, se añade un tinte soluble en agua a la emulsión. Si se trata de una emulsión aceite/agua, el medio de dispersión aparece rojo y la fase dispersa incolora y viceversa.
Separación de Emulsiones
Los distintos métodos por los que se pueden separar las emulsiones en sus líquidos constituyentes son los siguientes:
- Calentamiento
- Centrifugado
- Congelación, etc.
Aplicaciones y Usos de las Emulsiones
Las emulsiones son muy conocidas en diversos campos de la ciencia. Se utilizan en las industrias del curtido y el tinte, en el proceso de fabricación de plásticos y caucho sintético, etc.
- Suelen utilizarse en cosmética, farmacia e higiene personal.
- Las microemulsiones se utilizan para administrar vacunas que eliminan diversos microbios.
- Se utiliza en síntesis química, principalmente en la fabricación de dispersiones de polímeros.
- Se utiliza en la lucha contra incendios.
- Las nanoemulsiones, como el aceite de soja, se utilizan para matar microbios.
- La mayonesa es una emulsión de aceite en agua con yema de huevo o estearoil lactilato sódico.
Preguntas Frecuentes
No, las emulsiones son una mezcla coloidal no homogénea de dos líquidos inmiscibles.
La mantequilla es un ejemplo de emulsión.
Los dos tipos de emulsión son los siguientes: Emulsión de agua en aceite y Emulsión de aceite en agua
Un emulsionante es una sustancia que estabiliza las emulsiones.
Sí, los emulgentes son solubles en agua.
